Matrice de reconstruction tissulaire NovoMatrix®
Une option thérapeutique alternative à la greffe de tissu conjonctif
NovoMatrix® est une matrice dermique acellulaire produite à partir de derme porcin. Utilisée en chirurgie, la matrice résistante au déchirement et facile à utiliser1,2 représente une très bonne alternative à la greffe de tissu conjonctif (GTC) autologue. Elle permet d’éviter un prélèvement chirurgical intraoral, ce qui réduit la morbidité pour le patient.
Étant donné son processus de fabrication, la matrice ne contient pas de cellules du donneur. En outre, la structure du tissu d’origine reste pratiquement inchangée ce qui contribue à la croissance des cellules et des micro-vaisseaux. Grâce au conditionnement en douceur, le traitement exclusif des tissus permet une repopulation cellulaire et une revascularisation optimale, ce qui offre une régénération tissulaire esthétique.3 La matrice NovoMatrix® est fournie pré-hydratée, dans une solution aqueuse tamponnée au phosphate breveté contenant des stabilisateurs matriciels, et peut donc être utilisée rapidement sans réhydratation complexe.4
NovoMatrix® – Convient de manière optimale aux indications suivantes⁴
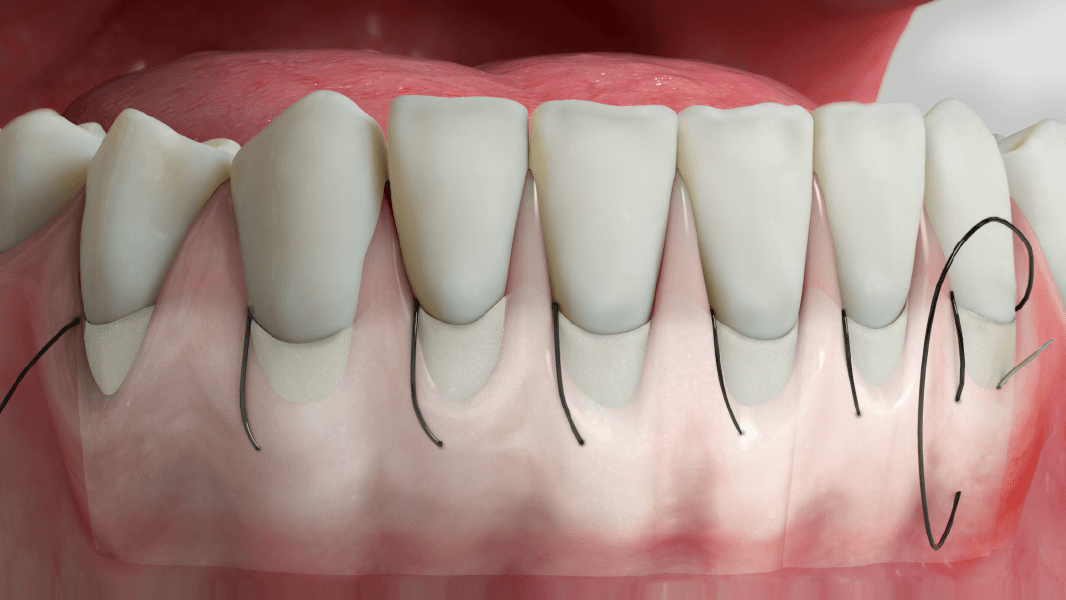
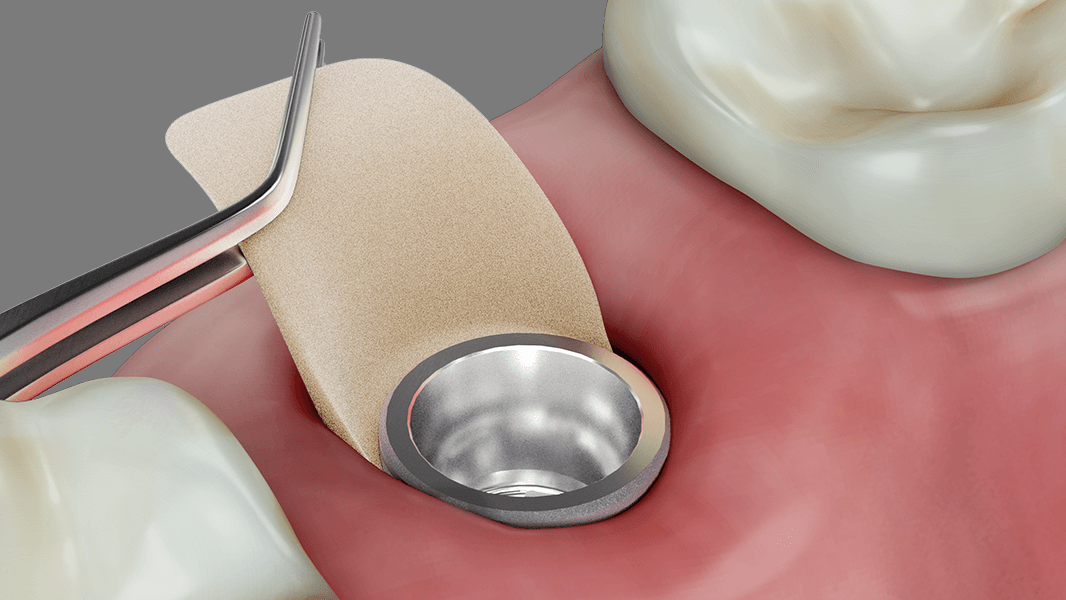
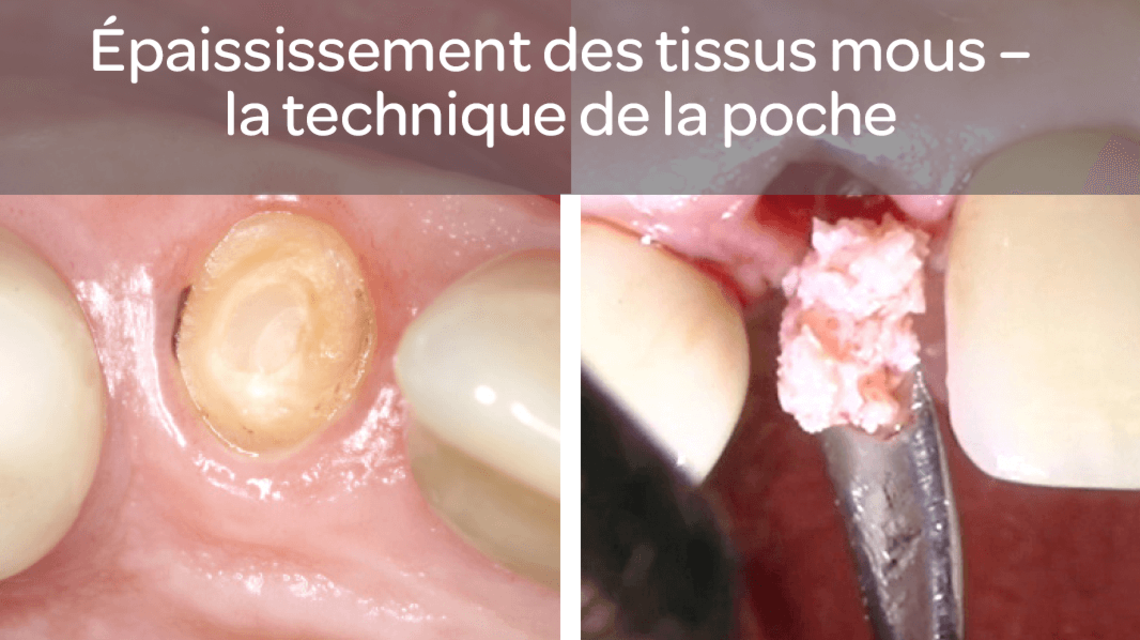
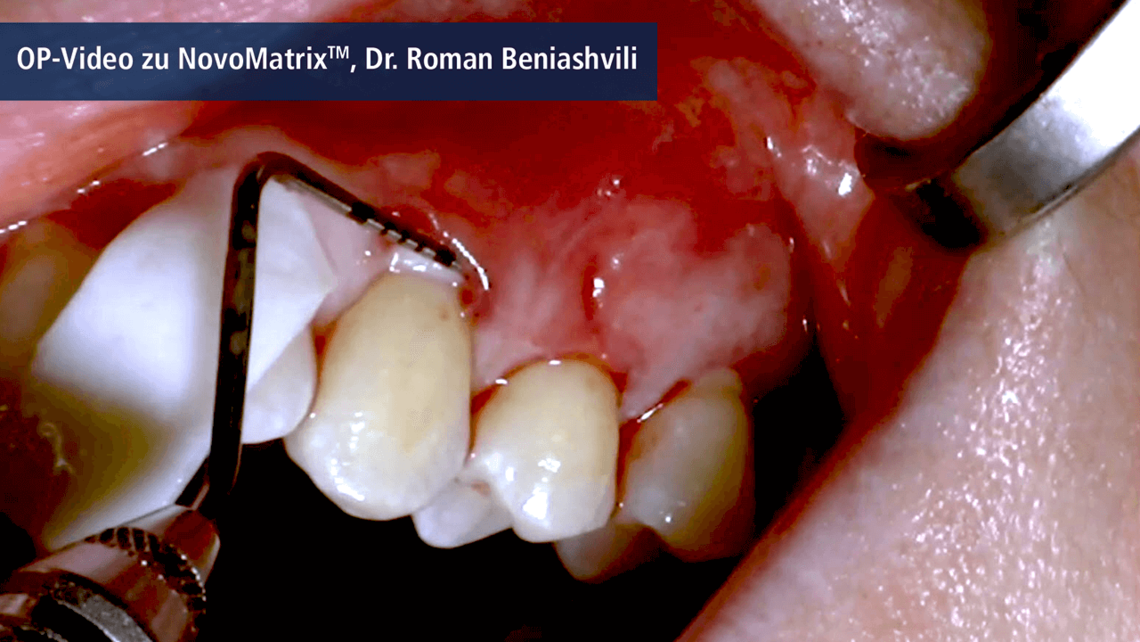
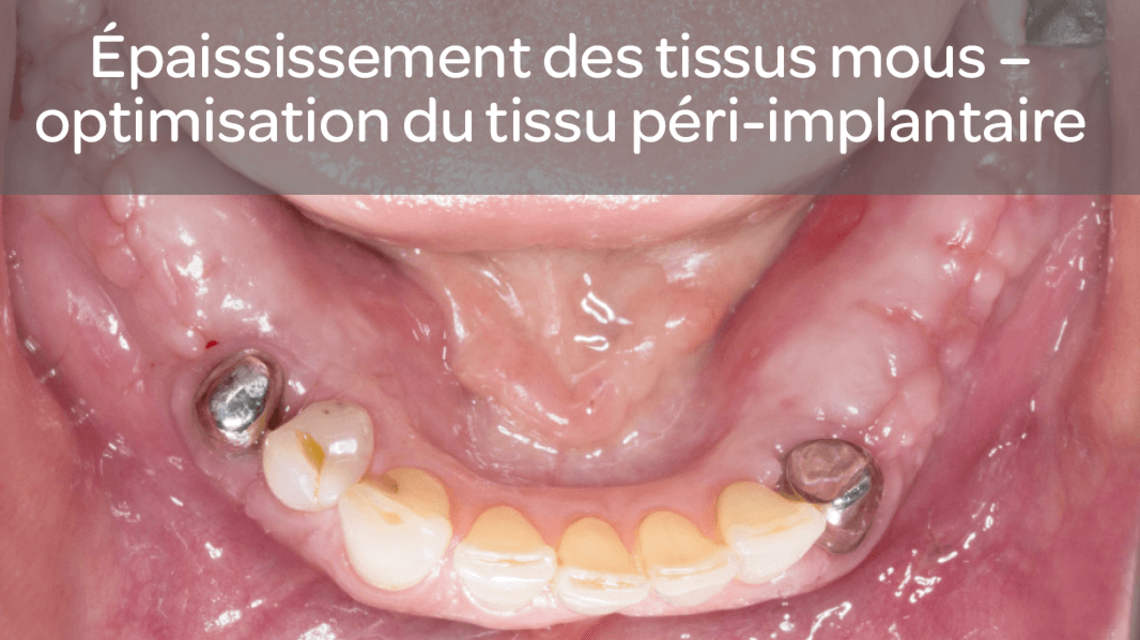
- Augmentation du tissu attaché autour des dents et des implants
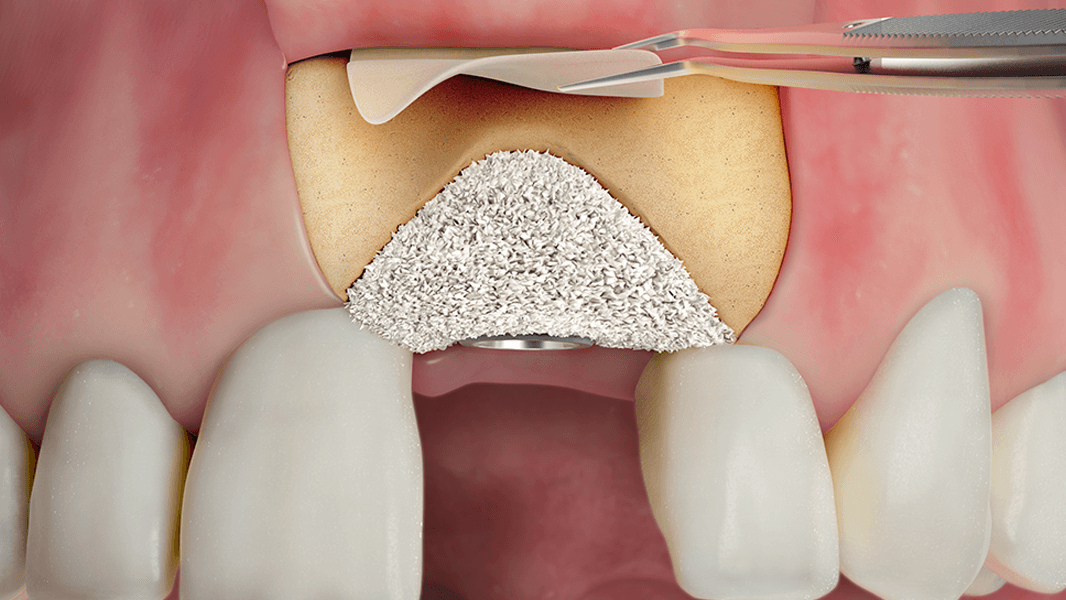
- Reconstruction de la crête alvéolaire pour la restauration prothétique
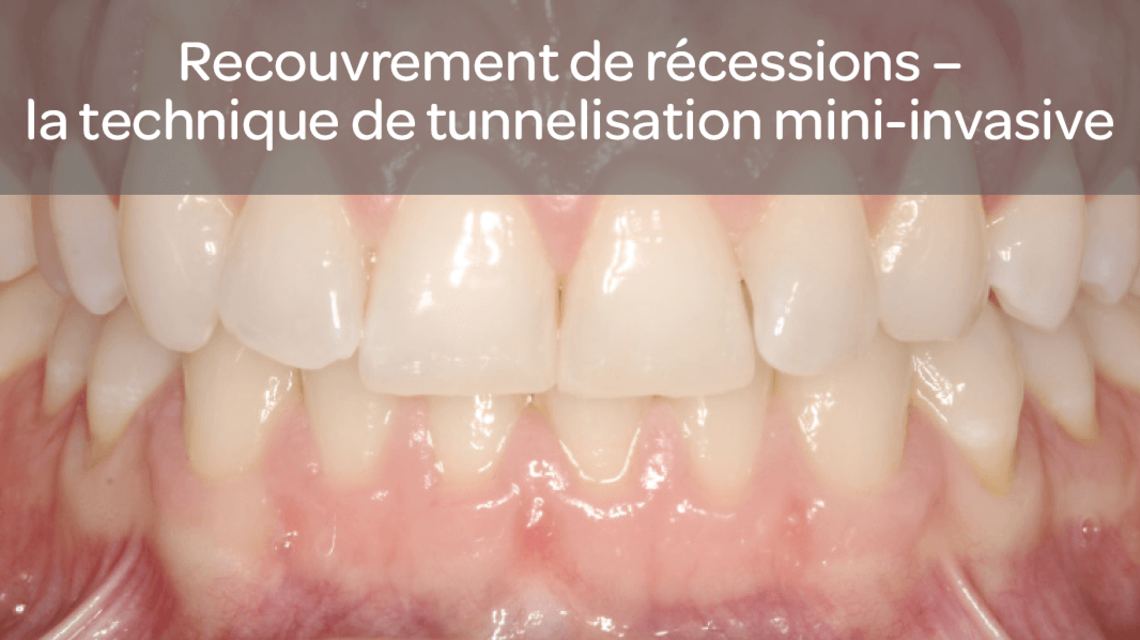
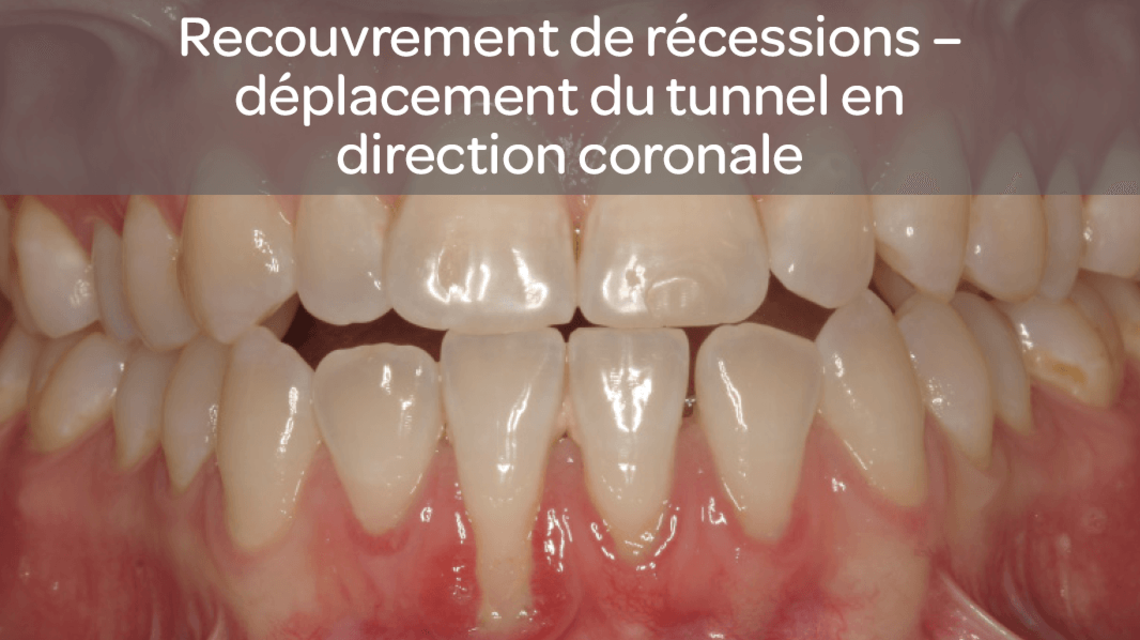
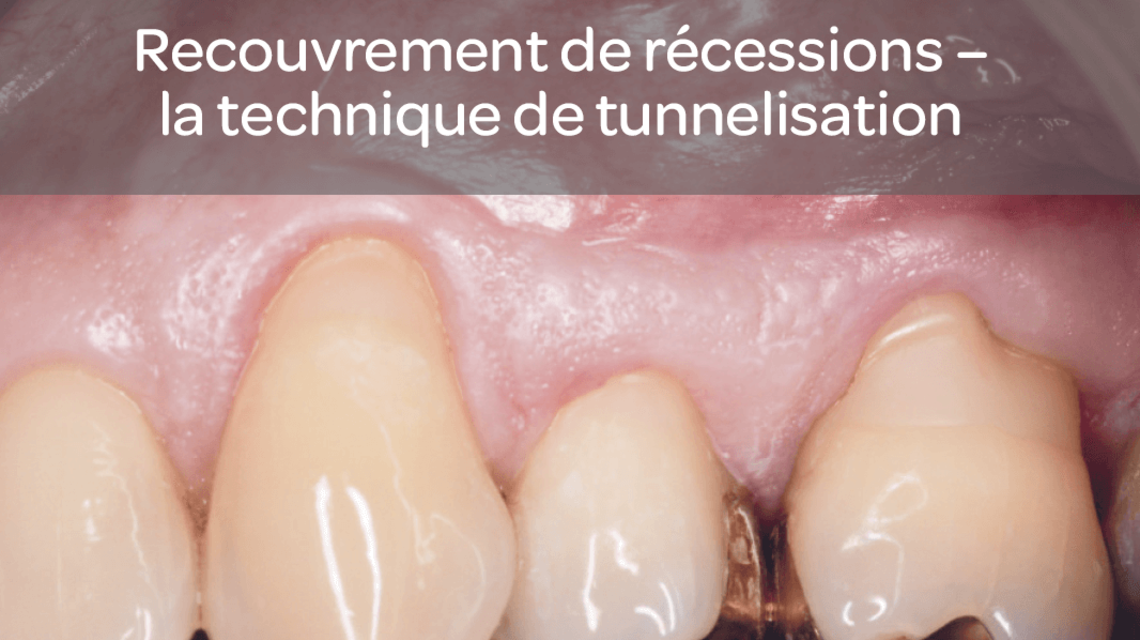
- Régénération tissulaire guidée en cas de défauts de récession pour le recouvrement radiculaire
Les caractéristiques de la matrice NovoMatrix®
- Le procédé de préparation des tissus LifeCell™ entraîne une revascularisation rapide.
- Épaisseur toujours égale des tissus
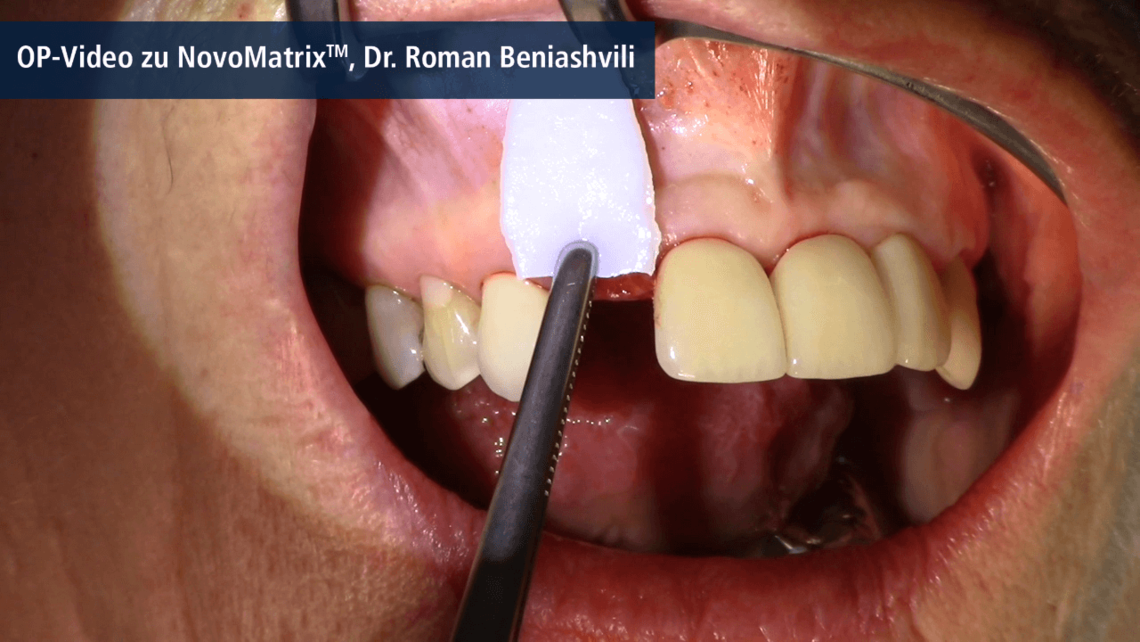
- Pré-hydratée – prête à l’emploi après la sortie de l’emballage et un bain de 2 minutes dans une solution saline stérile ou une solution ringer lactate4
- Conservation entre -8 °C et +30 °C4
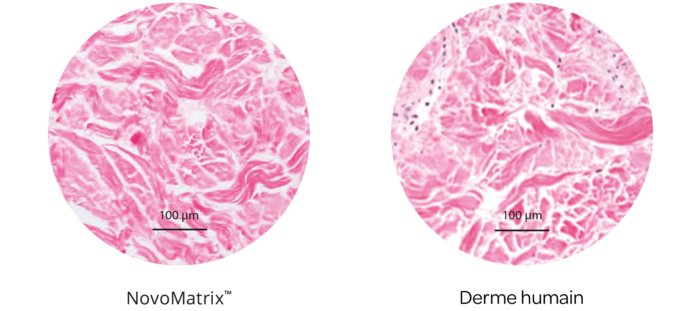
La structure tissulaire de NovoMatrix®
Maintien de la structure par un processus de fabrication exclusif
Le maintien de l’intégrité tissulaire est d’une importance essentielle pour atteindre des résultats biologiques efficaces. Les tissus originels sont donc traités avec douceur dans le cadre du processus de fabrication exclusif de la matrice NovoMatrix® afin d’assurer la préservation des tissus qui est décisive pour le maintien de leur intégrité biochimique et biomécanique.
Avantages de l'utilisation de la matrice NovoMatrix®
Acceptation élevée par les patients – durée de traitement réduite
- Réduction du temps opératoire
La matrice dermique acellulaire, rapidement prête à l’emploi, raccourcit le temps opératoire en évitant une deuxième intervention chirurgicale pour retirer une greffe de tissu conjonctif autologue.9
- Réduction de la morbidité du patient
Renoncer à un site de prélèvement palatin élimine la douleur postopératoire liée à la deuxième intervention.9,10,11
- Très bonne intégration tissulaire
L’utilisation de la matrice NovoMatrix® contribue à une revascularisation rapide ainsi que la recolonisation cellulaire et minimise la réaction inflammatoire.3,8,12,13
- Structure naturelle des tissus et de la couleur
L’utilisation de la matrice NovoMatrix® montre une très bonne cicatrisation et une très bonne adaptation de la structure des tissus et de la couleur aux tissus naturels environnants.14
- Cicatrisation rapide et sans complications des tissus mous
L’utilisation de la matrice NovoMatrix® contribue à la réaction immunologique positive ainsi qu’à l’intégration et la régénération tissulaire.3,12,13,15
LifeCell™ – plus de 25 ans d'expérience
Produits innovants pour la reconstruction tissulaire
Depuis plus de deux décennies, LifeCell™ développe des produits innovants pour un large spectre d’applications. Avec plus de 2,5 millions de greffons à ce jour, 25 ans d’expérience dans le traitement des tissus et une soif d’innovation permanente, LifeCell™, en collaboration avec BioHorizons et Camlog, a introduit dans la dentisterie NovoMatrix®, le matériau de nouvelle génération pour l’augmentation des tissus mous.

Littérature
Adsorption and Release of Growth Factors from Four Different Porcine-Derived Collagen Matrices
Enhanced Wound Healing Potential of Primary Human Oral Fibroblasts and Periodontal Ligament Cells Cultured on Four Different Porcine-Derived Collagen Matrices
Comparison of two soft tissue substitutes for the treatment of gingival recession defects: an animal histological study
Références
| 1 | Data on file, Allergan. NovoMatrix® – Mechanical testing, Preclinical Data. |
| 2 | Data on file, Allergan. INT/0204/2018. |
| 3 | Suárez-López Del Amo F, Rodriguez JC, Asa‘ad F, Wang HL. Comparison of two soft tissue substitutes for the treatment of gingival recession defects: an animal histological study. J Appl Oral Sci., 2019;27:e20180584. |
| 4 | Reference manufacturer’s Instructions for Use (IFU) package insert. |
| 5 | Necas J, Bartosikova L, Brauner P, Kolar J. Hyaluronic acid (hyaluronan): a review. Vet Med. 2008;53(8):397-411. |
| 6 | Ludwig MS. Proteoglycans and pathophysiology. J Appl Physiol. 2007;103:735-736. |
| 7 | Pankov R, Yamada KM. Fibronectin at a glance. J Cell Sci. 2002;115:3861-3863. |
| 8 | Harper JR, McQuillan DJ. Extracellular wound matrices: a novel regenerative tissue matrix (RTM) technology for connective tissue reconstruction. Wounds. 2007;19(6):163-168. |
| 9 | Griffin T, Cheung W, Athanasios Z, Damoulis P. Postoperative Complications Following Gingival Augmentation Procedures. J Periodontology 2006;77:2070-2079. |
| 10 | Aguirre-Zorzano LA, García-De La Fuente AM, Estefanía-Fresco R, Marichalar-Mendía X. Complications of harvesting a connective tissue graft from the palate. A retrospective study and description of a new technique. J Clin Exp Dent. 2017;9(12):e1439-45. |
| 11 | Tavelli L, Asa’ad F, Acunzo R, Pagni G, Consonni D, Rasperini G. Minimizing Patient Morbidity Following Palatal Gingival Harvesting: A Randomized Controlled Clinical Study. The International Journal of Periodontics & Restorative Dentistry 38(6):e127-e134 November 2018. |
| 12 | Sandor M, Leamy P, Assan P, et al. Relevant in vitro predictors of human acellular dermal matrix-associated inflammation and capsule formation in a nonhuman primatesubcutaneous tissue expander model. Eplasty. 2017;17:e1-e21. |
| 13 | Xu H, Wan H, Sandor M, et al. Host response to human acellular dermal matrix transplantation in a primate model abdominal wall repair. Tissue Eng Part A. 2008;14(2):2009-2019. |
| 14 | Van Orten A. Peri-implant thickening of soft tissue – stable and functional. Implantologie Journal 5 |
| 15 | Sandor M, Xu H, Connor J, et al. Host response to implanted porcine-derived biologic materials in a primate model of abdominal wall repair. Tissue Eng Part A.2008;14(12):2021-2031. |
| 16 | Data on file, Allergan. LRD2011-08-015. |
| 17 | Data on file, Allergan. LRD2013-02-004. |